Estudio en ratones encuentra que un fármaco contra el cáncer puede funcionar en enfermedades cerebrales comunes

Los investigadores del Centro Médico de la Universidad de Georgetown descubrieron que el fármaco previene la acumulación de proteínas tóxicas relacionadas con la enfermedad de Parkinson en el cerebro de los ratones. Los investigadores ahora desarrollarán un ensayo clínico para estudiar los efectos del fármaco en los seres humanos.
Los investigadores dicen que su estudio, publicado en línea en Genética molecular humana, es una nueva estrategia para el tratamiento de enfermedades neurodegenerativas que presentan una acumulación anormal de proteínas.
Las enfermedades comunes que se desarrollan en asociación con la acumulación anormal de proteínas incluyen la enfermedad de Parkinson, la enfermedad de Alzheimer, la esclerosis lateral amiotrófica (ELA), la demencia frontotemporal, la enfermedad de Huntington y la demencia con cuerpos de Lewy, entre otras.
"Este fármaco, en dosis muy bajas, enciende la maquinaria de eliminación de basura dentro de las neuronas para eliminar las proteínas tóxicas de la célula", dijo el investigador principal del estudio, el neurocientífico Charbel E-H Moussa, M.B., Ph.D.
"Al eliminar las proteínas intracelulares, el fármaco previene su acumulación en inclusiones patológicas llamadas cuerpos de Lewy y / o ovillos, y también previene la secreción de amiloide en el espacio extracelular entre las neuronas, por lo que las proteínas no forman grupos o placas tóxicas en el cerebro", dijo. .
Cuando el medicamento, nilotinib, se usa para tratar la leucemia mielógena crónica (LMC), obliga a las células cancerosas a la autofagia, un proceso biológico que conduce a la muerte de las células tumorales en el cáncer.
“Las dosis utilizadas para tratar la CML son lo suficientemente altas como para que el fármaco empuje a las células a masticar sus propios orgánulos internos, lo que provoca la autocanibalización y la muerte celular”, dijo Moussa.
“Razonamos que pequeñas dosis, para estos ratones, un equivalente al uno por ciento de la dosis utilizada en humanos, activarían la suficiente autofagia en las neuronas para que las células eliminen las proteínas que funcionan mal, y nada más”.
Moussa planteó la hipótesis de que los medicamentos contra el cáncer podrían ayudar a limpiar cerebros enfermos. "Nadie ha intentado algo como esto antes", dijo.
Sin embargo, una característica única del cerebro es una membrana que separa la sangre circulante del líquido extracelular del cerebro (BECF) en el sistema nervioso central (SNC).
Esta barrera hematoencefálica protege al cerebro de muchas infecciones bacterianas comunes, pero también ha limitado históricamente la administración de agentes médicos y terapéuticos.
Con este fin, Moussa y su equipo buscaron medicamentos contra el cáncer que pudieran atravesar la barrera hematoencefálica.
Descubrieron dos candidatos: nilotinib y bosutinib, que también están aprobados para tratar la CML. Este estudio analiza los experimentos con nilotinib, pero Moussa dice que el uso de bosutinib también es beneficioso.
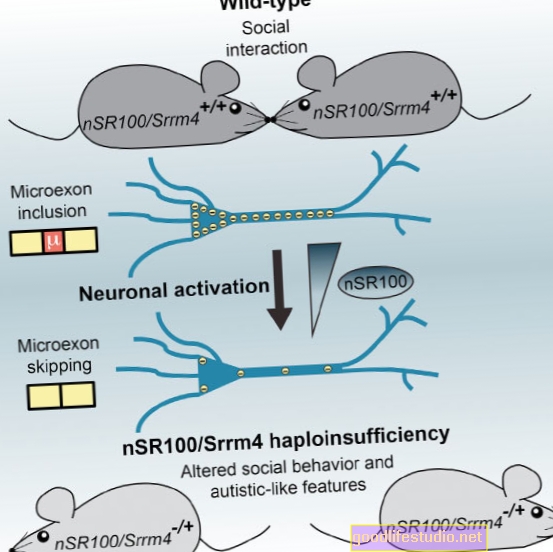
Los ratones utilizados en este estudio fueron modificados genéticamente para tener los cuerpos de Lewy que se encuentran en los pacientes con enfermedad de Parkinson y demencia, y en muchas otras enfermedades neurodegenerativas.
Los animales recibieron un miligramo de nilotinib cada dos días. (Por el contrario, la FDA aprobó el uso de hasta 1,000 miligramos de nilotinib una vez al día para pacientes con CML).
"Probamos con éxito esto para varios modelos de enfermedades que tienen una acumulación de proteína intracelular", dice Moussa. "Elimina la alfa sinucleína y la tau en varios trastornos del movimiento, como la enfermedad de Parkinson y la demencia con cuerpos de Lewy".
El equipo también mostró que el movimiento y la funcionalidad en los ratones tratados mejoraron enormemente, en comparación con los ratones no tratados.
Para que una terapia de este tipo tenga el mayor éxito posible en los pacientes, el agente debería usarse temprano en las enfermedades neurodegenerativas, dijo Moussa. El uso posterior podría retrasar la formación de placas extracelulares y la acumulación de proteínas intracelulares en inclusiones como los cuerpos de Lewy.
Moussa está planeando un ensayo clínico de fase II en participantes que han sido diagnosticados con trastornos que presentan acumulación de alfa sinucleína, incluida la demencia con cuerpos de Lewy, la enfermedad de Parkinson, la parálisis supranuclear progresiva (PSP) y la atrofia multisistémica (MSA).
Fuente: Centro Médico de la Universidad de Georgetown
























.jpg)
